Primeira dose foi aplicada em profissional de saúde da Capital nesta terça; doses devem chegar nesta semana na Famerp,
um dos 12 centros do País a testar o imunizante produzido na China
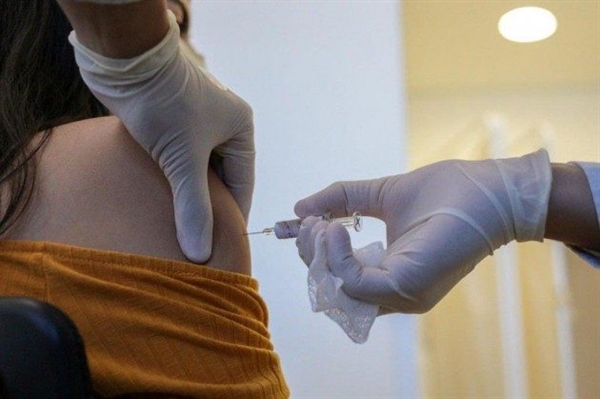
Médica toma a primeira dose da vacina nesta terça-feira, 21, em São Paulo (Foto: Divulgação/Governo de SP)
A Faculdade de Medicina de Rio Preto (Famerp) deverá testar a vacina contra o coronavírus em cerca de 500 voluntários. Os imunizantes e placebos que serão utilizados no ensaio clínico foram recebidos pelo Instituto Butantan nesta segunda-feira, 20. O estudo é uma parceria com a farmacêutica Sinovac Life Science, da China. O objetivo desta fase de testes é comprovar se o produto é ecaz e seguro.
Por enquanto, a parceria é entre Famerp, Instituto Butantan e a empresa chinesa e não envolve a Secretaria de Saúde de Rio Preto. Entre os recrutados, metade receberá duas doses do imunizante num intervalo de 14 dias e a outra metade receberá duas doses de placebo, uma substância com as mesmas características físicas, mas sem efeito. O voluntário não saberá qual está recebendo.
A CoronaVac é produzida com fragmentos desativados do coronavírus e, com a aplicação, o sistema imunológico passaria a produzir anticorpos contra o agente causador da Covid-19. Os voluntários serão monitorados pelos centros de pesquisa, assim será possível vericar se quem tomou a vacina cou protegido em relação a quem tomou o placebo.
Além da Famerp, outros onze centros no País serão responsáveis pelo estudo, que abrangerá 9 mil pessoas nos Estados de São Paulo, Minas Gerais, Rio de Janeiro, Distrito Federal, Paraná e Rio Grande do Sul. A médica Stefania Teixeira Porto, de 27 anos, que atua no Hospital das Clínicas, em São Paulo, foi a primeira voluntária a receber a dose, na manhã desta terça-feira, 21.
Depois da vacinação, ela foi submetida a vários testes e passou um período em observação no próprio Hospital das Clínicas, centro do estudo clínico no País. Por causa do desgaste físico, ela cancelou uma entrevista coletiva e enviou uma mensagem de vídeo por meio da Secretaria Estadual de Saúde.
"Estou contente de participar dessa experiência. É um momento único e histórico. Foi isso que me fez participar desse projeto e fazer parte desse momento. A gente passou por meses tão difíceis. É uma injeção de ânimo poder participar disso e contar para as pessoas no futuro que eu z parte disso", armou a médica.
Ao menos 900 interessados se candidataram até esta terça-feira, 21, para os testes da vacina chinesa contra a Covid-19 no Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo (USP) em Ribeirão Preto. Destes, serão selecionados os 300 voluntários que receberão a primeira dose da vacina na próxima semana. Questionados, nem Instituto Butantan nem Famerp informaram o número de voluntários no centro de Rio Preto.
Podem se candidatar para serem voluntários no estudo prossionais de saúde que estejam trabalhando no atendimento a pacientes com Covid-19 e que não tenham sido infectados pelo coronavírus nem tenham participado de outros estudos. Mulheres não podem estar grávidas nem planejando engravidar nos próximos três meses. Outra restrição é não ter doenças instáveis ou fazer uso de medicações que alterem a resposta imune.
As inscrições devem ser feitas em https://www.saopaulo.sp.gov.br/coronavirus/vacina. No site, o candidato pode responder a algumas perguntas e vericar se tem o perl necessário. As informações coletadas são sigilosas.
(Com Agência Estado)
Anvisa aprova novo ensaio
A Agência Nacional de Vigilância Sanitária (Anvisa) informou ter aprovado a condução de um ensaio clínico que estudará outros dois tipos de vacinas contra a Covid-19. Essas vacinas estão sendo desenvolvidas pelas empresas BioNTech e Pzer e são baseadas em ácido ribonucleico (RNA), que codica um antígeno especíco do vírus.
Segundo a agência, o estudo prevê a inclusão de cerca de 29 mil voluntários. Desse total, 5 mil são no Brasil, distribuídos nos Estados de São Paulo e Bahia.
Este é o terceiro estudo de vacina contra o novo coronavírus autorizado pela Anvisa no Brasil. No dia 2 de junho, o órgão liberou o ensaio clínico da vacina desenvolvida pela Universidade de Oxford, no Reino Unido, e, no dia 3 de julho, o da vacina desenvolvida pela empresa Sinovac, em parceria com o Instituto Butantan.
Em nota, a Anvisa informou que, para a autorização dada nesta terça-feira, 21, foram analisados os dados das etapas anteriores de desenvolvimento dos produtos e os "resultados obtidos até o momento demonstraram um perl de segurança aceitável das vacinas candidatas".
*Diário da Região










